主任教授 岡 三喜男
我々は、世界で初めて「肺がんにおいて恒常的な免疫監視機構の存在」を証明した(1)。また、その免疫反応の強弱が肺腺がんの予後を決定していることを臨床的に明らかにした(2,3)。肺がんのがん抗原特異的な腫瘍免疫の詳細な解析は、我々のXAGE1関連研究の成果が最初で唯一です。その最大の理由は、「肺がん特異的ながん抗原」が同定されていなかったからです。この「がん精巣抗原XAGE1」は、肺がんで最も多い肺腺がんに高率に発現し、強い免疫原性を有しているため、とくに肺がんの免疫学的解析のバイオマーカーや治療の標的として極めて有用です。これらの成果は、現在の免疫チェックポイント阻害薬の肺がんに対する臨床的な効果を裏付けるものです。
- Ohue Y, Eikawa S, Okazaki N, Mizote Y, Isobe M, Uenaka A, Fukuda M, Old LJ, Oka M, Nakayama E. Spontaneous antibody, and CD4 and CD8 T-cell responses against XAGE-1b (GAGED2a) in non-small cell lung cancer patients. Int J Cancer 131(5):E649-58, 2012
- Ohue Y, Kurose K, Mizote Y, Matsumoto H, Nishio Y, Isobe M, Fukuda M, Uenaka A, Oka M, Nakayama E. Prolongation of overall survival in advanced lung adenocarcinoma patients with the XAGE1 (GAGED2a) antibody. Clin Cancer Res 20(19):5052-63, 2014 Selected in the "Highlight" section (Oct 1, 2014)
- Ohue Y, Wada H, Oka M, Nakayama E. Antibody response to cancer/testis (CT) antigens: A prognostic marker in cancer patients. OncoImmunology 3(11):e970032-33, 2014
【肺がんの免疫監機構】
一般に「がん」の定義は、正常細胞に遺伝子異常が蓄積し、その細胞は形質転換して無限に増殖して、臨床的には転移や臓器の破壊を来たし、最終的には宿主であるヒトを死に至らしめる。したがって、がんの征服には基礎的かつ臨床的な知識と理解が必要である。
「免疫」は本来、疫病から生体が免れる事に語源を発し、外来および内在抗原に対する特異的な宿主反応である。しかし腫瘍免疫はがん特異的抗原(がん抗原)が特定されず約130年間、病理的、実験的、疫学的解析から腫瘍炎症として捉えられてきた。確かに多くの腫瘍内には、リンパ球を中心とした炎症細胞浸潤がみられ、腫瘍の進展に免疫の関与が強く示唆される。
免疫は、常に遺伝子異常を蓄積した異常細胞を非自己と認識し排除している(Burnetの免疫監視機構)。一般にヒトでは毎日、数千のがん細胞が発生し、この免疫監視機構によって、がん細胞は排除されていると言われている。しかし一部の異常細胞は免疫監視から免れ、免疫とがん細胞の力関係が平衡状態になるが、腫瘍関連サイトカインや免疫チェックポイント分子などの免疫抑制因子の発現によって、最終的に異常細胞は免疫監視から逃れ進行がんとなる(がん免疫編集の概念)。
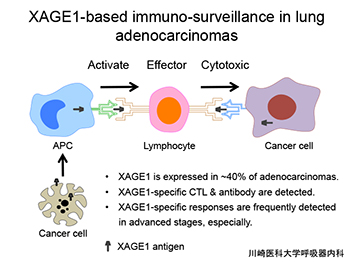
「がん」において、免疫監視機構の存在を証明するには、がん組織からがん抗原を同定し、それに対する特異的な抗体と細胞傷害性Tリンパ球(CTL)の両者を検出することが求められる。当に、我々のXAGE1抗原こそがこの定義を満たすものである(上図)。
【がん抗原】
では免疫は、何を目印にしてがん細胞と認識し排除しているのか?
この長年の大命題に対し1991年、遂にThierry Boonらは悪性黒色腫からヒトがん特異抗原のMAGE-A1(melanoma-associated antigen-A1)とそれを認識するCTLを同定し、リンパ球を介した抗腫瘍免疫機構を確立し、腫瘍免疫学は大きな一歩を踏み出した。その後、SEREX法の開発によって、NY-ESO-1(New York esophageal squamous cell carcinoma-1)やMAGE-A3に代表されるがん精巣抗原(CT, cancer/testis antigen)が続々と同定された。それ以来、我々も長年、肺腺がんに発現するCT抗原XAGE1について研究している。
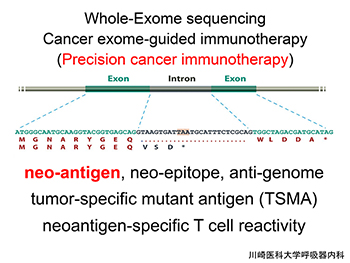
現在、がん関連抗原は次のように分類され、①ウィルス発がん蛋白(例:E6、E7)、②過剰発現蛋白(例:HER2/neu)、③がん遺伝子変異蛋白(例:RAS、TP53)、④分化抗原(例:CD20)、⑤融合遺伝子蛋白(例:BCR-Abl)、⑥がん精巣抗原(CT抗原)、⑦全エキソーム解析による変異ペプチドのneoantigen(neoepitope, mutanome, TSMA)、これら多数の抗原について臨床検体での発現と液性または細胞性免疫応答の解析が精力的に展開されている。最近、とくにneoantigenは個別化免疫療法の先導役として最も注目され(下図)、我々もこの分野への参入を開始しているが、肺がんについては唯一、XAGE1抗原のみモニター解析ができる。
【がん精巣抗原】
がん精巣抗原(CT抗原)は、当初その発現解析からがん細胞と正常の精巣組織に限局して発現していたことから、がん精巣抗原と呼ばれるようになった。現在、約225遺伝子がその発現形式からCT遺伝子とされているが、一部を除いて免疫学的な抗原性については不明であるため、厳密にはCT遺伝子とCT抗原は区別している。その後の遺伝子解析からCT遺伝子はX性染色体上に存在するCT-X遺伝子と、常染色体上にあるnon-CT-X遺伝子に分類された。non-CT-X遺伝子は他の正常組織にも広く発現するため、がん特異的な研究や治療ワクチンにはCT-X遺伝子が適している。一般にCT-X遺伝子はコピー数も多く、正常精巣の精原細胞や各種のがん組織に発現が高く抗原性も高い、一方、non-CT-X遺伝子は広く組織分布して精子形成の後期に発現する。
以上の事実から、CT-X遺伝子は人類が子孫を残すための基本に関わる、細胞を無限に増やす機能を担っていると考えられる(私見)。したがって、無限に増殖するがん細胞でのCT-X遺伝子の発現は当然であり、我々のXAGE1の臨床的解析でも肺腺がんの予後不良因子になっている(下図)。
文献)岡 三喜男、大植祥弘、黒瀬浩史、中山睿一:がん精巣抗原に対する免疫応答とその臨床的意義. BIO Clinica 30(30):31-35,2015
【がん精巣抗原と免疫応答】
腫瘍免疫学において、がん抗原の発現解析とそれに対する特異的な免疫応答の検出は最も基本的な事項である。上述のがん抗原①~⑦の中で、明確な液性および細胞性免疫応答を検出した報告は極めて少ない。例えばTP53のように広範ながん種で高率に変異蛋白の発現をみるが、血清抗体は検出しても特異的CTLの誘導を証明した報告は無く(split immune tolerance)、検出する技術的かつ精度的な問題は別にしても多くのがん抗原も同様である。
一方、正常の精巣組織はMHC-class 1(MHC-1)を発現していないため免疫原性はないが、CT抗原の中で我々のXAGE1、他にMAGE-A1、MAGE-A3、NY-ESO-1、SSXにおいてのみ、がん患者から液性免疫と細胞性免疫応答を検出している。
我々は肺がんで最も頻度の高い肺腺がんでXAGE1に対する強い免疫応答の存在を明らかにしている(上図)。CT-X抗原であるXAGE1は、肺腺がんの約40%に発現し、抗原発現者の約半数に抗XAGE1血清抗体を検出している。また抗XAGE1血清抗体陽性者でXAGE1特異的なCTLの誘導を高頻度に認めた。これまでの我々の経験から、CT-X抗原であるXAGE1とNY-ESO-1は、強い免疫原性を誘導し抗腫瘍免疫に深く関与していると考えられるが、残念なことに肺がんにおけるNY-ESO-1の発現頻度は約5%に過ぎない。
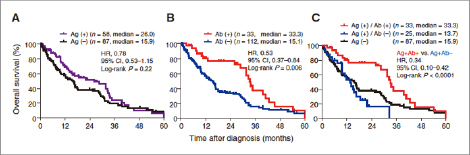
一方、これら概念的な免疫編集が肺がん患者において成立するか不明であった。我々は、肺腺がんに高頻度に発現するがん特異抗原XAGE1を指標として、免疫能を網羅的に解析し、進行期でもXAGE1に対する抗腫瘍反応が持続していることを明らかにした。さらに抗XAGE1血清抗体を有する患者は抗体陰性に比べ予後が延長する事を見いだした(下図)。これらの研究成果は肺がんの免疫監視機構の恒常性を実証し、免疫抑制解除によって必然的に抗腫瘍反応が増強することを示唆している。つまり今日の免疫チェックポイント阻害薬の有効性を支持する重要な根拠となった。
- Ohue Y, Kurose K, Mizote Y, Matsumoto H, Nishio Y, Isobe M, Fukuda M, Uenaka A, Oka M, Nakayama E. Prolongation of overall survival in advanced lung adenocarcinoma patients with the XAGE1 (GAGED2a) antibody. Clin Cancer Res 20(19):5052-63, 2014
Selected in the “Highlight” section of Clinical Cancer Research (Oct 1, 2014) - Pandey JP, Namboodiri AM, Ohue Y, Oka M, Nakayama E. Genetic variants of immunoglobulin g and k chains influence humoral immunity to the cancer-testis antigen XAGE-1b (GAGED2a) in patients with non-small cell lung cancer. Clin Exp Immunol 176(1):78-83, 2014
【肺がんの免疫微小環境】
では何故、腫瘍は免疫によって拒絶されないのか?
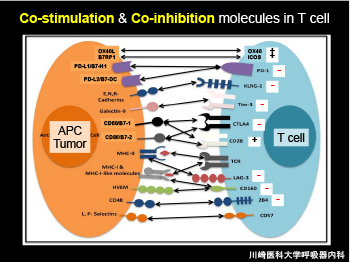
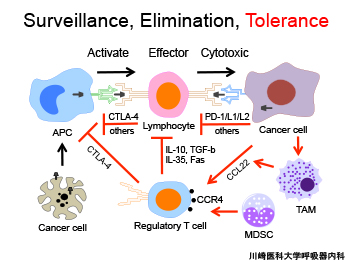
免疫監視機構は抗原を認識するとアクセルを踏み排除に向かって作動するが、免疫が過剰に反応するとサイトカイン・ストームや自己免疫疾患に代表される副反応が惹起される。このため免疫には、サイトカイン、細胞、および分子レベルでのアクセル(活性)とブレーキ(抑制)があり(下図)、その調整をするチェックポイント機構が存在する。例えば、健常人では感染症に対し、免疫はアクセルとブレーキの両者のバランスをとり宿主は治癒へと向かう。ブレーキ役としてのサイトカインではIL-10やTGFβ、細胞では制御性T細胞(Treg)や骨髄由来抑制細胞(MDSC)、分子ではCTLA-4やPD-1が代表格として挙げられる。
一方、進行がん局所の免疫微小環境では、常に抗腫瘍(アクセル)と抑制因子(ブレーキ)が混在し、がんの進行過程では抑制が優位に立っていることが推測される(がん免疫編集の概念)。主たる抑制因子としてTreg、MDSC、腫瘍関連マクロファージ2型(M2マクロファージ)、免疫チェックポイント分子(CTLA-4、PD-1/PD-L1/L2)など多数あり、これらは翻って免疫療法の標的でもある。
我々の研究室では、多数の臨床検体を解析し、肺がん局所に活性化したTregが集積し、その表面にはケモカイン受容体CCR4が高発現している事を報告した(1)(下図)。また抗CCR4抗体によるTregの除去を目的にした世界初の臨床試験を行った(2)。肺がん免疫微小環境には、PD-1/PD-L1経路を含めた多数の免疫制御因子が存在している(3)。
肺がんの免疫制御で重要なことは、全体を俯瞰しながら各因子を順次に解析し、最も鍵となるものを標的にして複合させることに尽きる。そのためには、眼前の分子にのみ固執すること無く、基本に立ち返って、生体の成り立ちと機能を理解しておく必要がある。
- Kurose K, Ohue Y, Sato E, Yamauchi A, Eikawa S, Isobe M, Nishio Y, Uenaka A, Oka M, Nakayama E. Increase of activated Treg in TIL in lung cancer and in vitro depletion of Treg by ADCC using an anti-human CCR4 mAb (KM2760). J Thorac Oncol 10(1):74-83, 2015
- Kurose K, Ohue Y, Wada H, Iida S, Ishida T, Kojima T, Doi T, Suzuki S, Isobe M, Funakoshi T, Kakimi K, Nishikawa H, Udono H, Oka M, Ueda R, Nakayama E. Phase Ia study of FoxP3+ CD4 Treg depletion by infusion of a humanized anti-CCR4 antibody, KW-0761, in cancer patients. Clin Cancer Res 21(19):4327-4336, 2015
Press Release by AACR, Am Asso for Cancer Res (Oct 1, 2015)
http://www.aacr.org/Newsroom/Pages/News-Release-Detail.aspx?ItemID=766#.Vg0u19RKOK0 - Ohue Y, Kurose K, Isobe M, Nishio Y, Tanaka T, Doki Y, Hori T, Fukuoka J, Oka M, Nakayama E. Survival prediction using immune parameters PD-L1, galectin-9 and XAGE1 (GAGED2a) expressed in the tumor cells, and tumor infiltrating T-cells, in lung adenocarcinoma patients. 2016 (submitted)
文責:主任教授 岡 三喜男
(2016.3.11)
(2016.3.11)